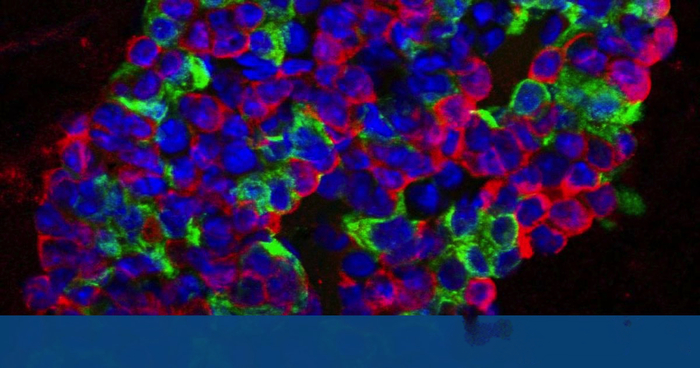
El mantenimiento postnatal o la regeneración de las células beta pancreáticas, se cree que se produce exclusivamente a través de la replicación de las células beta existentes, pero clínicamente la restauración de células beta humanas por replicación nunca se había logrado. Se ha descubierto una población de células beta inmaduras que está presente durante toda la vida y se forma a partir de precursores no beta, en un microambiente especializado o «nicho neogénico» en la periferia de los islotes de Langerhans. Estas células producen insulina, pero carecen de otros marcadores de células beta clave, y son transcripcionalmente inmaduras, incapaces de detectar la glucosa, y no pueden soportar la afluencia de calcio. Constituyen una etapa intermedia en la transdiferenciación de células alfa a células que son funcionalmente indistinguibles de las células beta convencionales. Por lo tanto, se ha identificado una fuente permanente de nuevas células beta en un sitio especializado dentro de islotes saludables. Al comparar las células beta inmaduras y maduras coexistentes dentro de islotes saludables, podemos aprender a hacer madurar células que produzcan insulina en células beta funcionales.
Intentaré explicarlo en un lenguaje más llano, ya que creo que es una noticia muy buena para la salud y para la ingeniería celular.
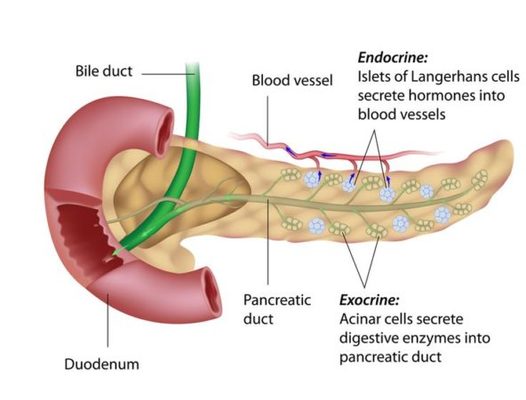
En las personas con diabetes tipo I, las células beta productoras de insulina en el páncreas mueren y no son reemplazadas. Sin estas células, el cuerpo pierde la capacidad de controlar la glucosa en la sangre. Investigadores de la Universidad de California en Davis han descubierto una posible nueva ruta para regenerar las células beta, dando una idea de los mecanismos básicos detrás del metabolismo saludable y la diabetes. Eventualmente, tal investigación podría conducir a un mejor tratamiento o cura de la diabetes.
«Hemos visto avances fenomenales en el tratamiento de la diabetes, pero no podemos curarla», afirmó Mark Huising, profesor asistente de neurobiología, fisiología y comportamiento en el Colegio Universitario de Ciencias Biológicas de la UC Davis. «Si quieres curar la enfermedad, tienes que entender cómo funciona en condiciones normales«.
Huising es autor principal en un artículo sobre el trabajo publicado el 4 de abril en la revista Cell Metabolism.
Trabajando con ratones de laboratorio y tejidos humanos, Huising está estudiando cómo las células de los islotes de Langerhans en el páncreas trabajan juntas para regular la glucosa en sangre. Tanto en ratones como en personas, los islotes contienen células beta, que detectan glucosa y secretan insulina, y otros tipos de células incluyendo las células alfa que producen glucagón, una hormona que eleva el azúcar en la sangre. Los efectos opuestos de la insulina y el glucagón permiten al cuerpo regular los azúcares en la sangre y almacenar los nutrientes.
La diabetes tipo I es una enfermedad con dos partes. En primer lugar, las células beta son destruidas por el propio sistema inmunológico del cuerpo, y luego no se regeneran (o las que se matan). Una cura efectiva para la diabetes tipo I implicaría tratar ambos problemas.
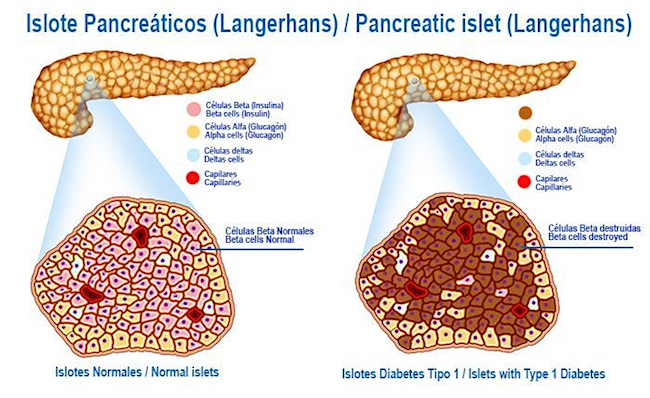
El dogma aceptado, dijo Huising, ha sido que las nuevas células beta son generadas por otras células beta que se dividen. Pero ahora, aplicando nuevas técnicas en microscopía, su equipo ha descubierto, dispersos alrededor de los bordes de los islotes, otro tipo de célula que se parece mucho a una célula beta inmadura.
Estas nuevas células pueden producir insulina, pero no tienen los receptores para detectar la glucosa, por lo que no pueden funcionar como una célula beta completa. Sin embargo, el equipo de Huising fue capaz de observar las células alfa en el islote se convierten en células beta inmaduras y luego madurar en células beta reales.
«Hay mucha más plasticidad en el sistema de lo que se pensaba«, comentó Huising.
Comprendiendo los Fundamentos del Metabolismo y la Diabetes
Es un resultado muy emocionante por tres razones, dijo Huising. En primer lugar, se trata de una nueva población de células beta en seres humanos y ratones que no se conocía antes. En segundo lugar, la nueva población podría ser una fuente para reponer las células beta muertas en la diabetes. Por último, la comprensión de cómo estas células maduran en células beta funcionales podría ayudar en el desarrollo de terapias con células madre para la diabetes. Las células madre tienen el potencial de desarrollarse en una amplia gama de otras células. Hasta ahora, los intentos de desarrollar verdaderas células beta de las células madre han hecho grandes progresos, pero estos esfuerzos aún no han alcanzado su máximo potencial porque se suspenden en una etapa inmadura anterior.
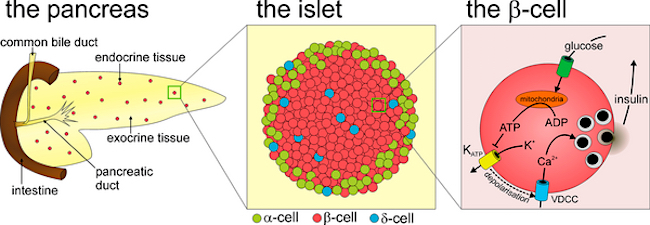
Esta comprensión básica de las células en los islotes también podría ayudar en la comprensión de la diabetes tipo II, donde las células beta no mueren, pero se vuelven inactivas y ya no secretan/liberan insulina.
«La JDRF se enorgullece de haber apoyado al Dr. Huising en este trabajo y está muy entusiasmada con los resultados mostrados en el documento.El concepto de aprovechar la plasticidad del islote para regenerar las células beta ha surgido como una intrigante posibilidad en los últimos años», dijo Andrew Rakeman, Ph.D., director de investigación del descubrimiento en JDRF. «El trabajo del Dr. Huising y de su equipo nos está mostrando no sólo el grado de plasticidad en las células de los islotes, sino también las trayectorias que toman estas células al cambian la identidad, agregando también, que las observaciones que los mismos procesos parecen estar ocurriendo en los islotes humanos hacen que exista la posibilidad de que estos conocimientos mecánicos puedan convertirse en enfoques terapéuticos para el tratamiento de la diabetes».